Forscher klären wichtigen Mechanismus für schnelle Kommunikation zwischen Nervenzellen auf
Blitzschnell auf einen Warnruf reagieren, mit dem Auto einem auf die Straße laufenden Kind ausweichen – solch rasche Reaktionen sind nur möglich, weil unsere Nervenzellen in Sekundenbruchteilen miteinander kommunizieren. Einen entscheidenden Mechanismus, der eine derart schnelle Signalübertragung erst möglich macht, haben jetzt Wissenschaftler aus Braunschweig und Göttingen aufgeklärt. (Nature Communications, 15. Dezember 2014)
Kommunikation ist nicht nur für unser Sozialleben unverzichtbar. Auch Zellen stehen pausenlos miteinander im Austausch, damit wir atmen, uns bewegen oder denken können. Einen Ball zu fangen wäre auch für Manuel Neuer undenkbar, könnten unsere Nervenzellen nicht innerhalb von Sekundenbruchteilen Informationen weiterleiten. Gewöhnlich werden diese Signale durch spezielle Botenstoffe übermittelt. Portionsweise verpackt liegen diese in kleinen Membranbläschen – den synaptischen Vesikeln – in einem Nervenende der Zelle bereit. Zeigen Signale an, dass eine Botschaft übermittelt werden soll, verschmelzen einige synaptische Vesikel mit der Zellmembran der sendenden Zelle und setzen ihre Botenstoffe frei. Diese lösen in der empfangenden Zelle ein Signal aus. Was diesen Prozess in Gang setzt, ist seit Langem bekannt: ein Anstieg der Kalziumionen-Konzentration im Nervenende der sendenden Zelle. Wie die Vesikel dieses Signal aber im entscheidenden Schritt erkennen und verarbeiten, um daraufhin sofort die Membranen zu verschmelzen, war bislang unklar.
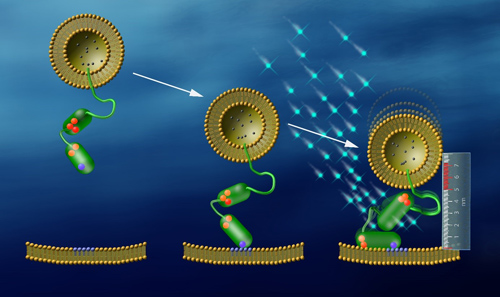
Mithilfe von Fluoreszenzsignalen und einem Nanolineal aus DNA konnten Peter J. Walla und seine Mitarbeiter genau beobachten, wie Synaptotagmin (grün) Vesikel an die Membran bindet. Mit einem Abstand von etwa acht Nanometern von der Membran befinden sich Vesikel in einer „Startposition“ für die Signalübertragung zwischen Nervenzellen. Steigt der Kalziumspiegel an, lagern sich Kalziumionen (hellblau) an das Synaptotagmin an, woraufhin dieses das Vesikel auf fünf Nanometer an die Membran heranzieht. Bei diesem Abstand können beide verschmelzen und die Botenstoffe freisetzen. Image credit: © Walla, Max-Planck-Institut für biophysikalische Chemie
Verschmelzen können die Vesikel mit der Membran der sendenden Zelle nur dann, wenn sich beide nahe genug kommen. Ein Team von Wissenschaftlern um Peter J. Walla von der Technischen Universität (TU) Braunschweig und dem Göttinger Max-Planck-Institut (MPI) für biophysikalische Chemie hat nun das Protein „bei der Arbeit“ beobachtet, das für diese enge Nachbarschaft sorgt. „Dieses Protein, Synaptotagmin genannt, bringt Vesikel und Membran genau auf die richtigen Abstände zusammen. Man kann sich Synaptotagmin als eine Art molekularen Anker vorstellen“, erklärt Peter J. Walla, Professor an der TU Braunschweig und Leiter der Forschungsgruppe Biomolekulare Spektroskopie und Einzelmoleküldetektion am MPI für biophysikalische Chemie.
Mit einem Ende ist Synaptotagmin im Vesikel fest verankert. Die Forscher konnten direkt verfolgen, wie es mit seinem anderen Ende an die Membran bindet und beide auf einem Abstand von etwa acht Nanometer (acht Millionstel Millimeter) hält. Bei diesem Abstand sind die Vesikel in „Startposition“ und sind jederzeit startklar. „Die Entfernung ist noch groß genug, um zu verhindern, dass Vesikel und Membran verschmelzen und die Botenstoffe freisetzen“, so Walla. Denn die sogenannten SNARE-Proteine auf dem Vesikel und der Membran, die für das Verschmelzen sorgen, müssen sich wie ein Reißverschluss ineinander verhaken. Und bei einer Entfernung von acht Nanometern kann sich dieser Reißverschluss nicht komplett verschließen.
Steigt nun die Kalziumkonzentration, ist das der Startschuss. „Das Kalzium lagert sich an Synaptotagmin an. Daraufhin ändert das Protein seine Form und zieht Vesikel und Membran auf fünf Nanometer zusammen. Das ist nah genug, damit die SNAREs sehr schnell für ein Verschmelzen sorgen können“, so der Chemiker. „Unsere Arbeit ist der erste Beweis überhaupt, dass Synaptotagmin aufgrund des Kalziums seine Form so ändert, dass sich der Abstand zwischen Vesikel und Membran genau im richtigen Maß verringert.“
Bisher waren alle Versuche, den genauen Abstand zwischen Vesikel und Zellmembran zu vermessen, schlicht am passenden Werkzeug gescheitert. Die Wissenschaftler um Walla waren nun erfolgreich, indem sie eine raffinierte neue Technik entwickelten: Sie nutzten DNA-Stränge genau bekannter Länge als eine Art Lineal im Nano-Maßstab. Indem sie Änderungen in der Leucht-Intensität und Dauer von Fluoreszenz-Signalen beobachteten, konnten die Forscher den Abstand von Vesikel und Membran auf den Nanometer genau bestimmen. „Der Ansatz, kurze Distanzen zwischen zwei einzelnen Punkten mithilfe von Fluoreszenzfarbstoffen zu messen, ist an sich nicht neu. Aber erst mithilfe der DNA-Stränge als Nanolineale konnten wir auch Abstände zwischen kompletten Membranflächen ausreichend genau ermitteln“, erläutert Chao-Chen Lin vom MPI für biophysikalische Chemie.
Das Nanolineal für Membranabstände ist nicht nur für die Neurobiologie ein vielversprechendes Werkzeug. Peter J. Walla ist überzeugt: „Bald könnte es auch in weiteren Forschungsvorhaben zum Einsatz kommen, denn Abstände zwischen Zellmembranen spielen auch bei ganz anderen biologischen Vorgängen eine Rolle, etwa, wenn Viren an eine Wirtszelle andocken oder bei der Befruchtung einer Eizelle.“
*Source: Max-Planck-Institut für biophysikalische Chemie
