Freiburger Forschungsteam entdeckt Grundlage für die Untersuchung zur Ausbreitung der Viren
Neue Erkenntnisse darüber, wie sich das Ebolavirus im menschlichen Körper ausbreitet: Einem deutsch-amerikanischen Forschungsteam ist es gelungen, Kanäle in intrazellulären Membranen zu identifizieren, die für den Virustransport entscheidend sind. Diese Kanäle können mit einem Wirkstoff blockiert werden, was im Tiermodell zu einem Stopp der Infektion führte. Die Ergebnisse veröffentlichten die Arbeitsgruppen um den Freiburger Pharmakologen Prof. Dr. Norbert Klugbauer, die Pharmakologen Prof. Dr. Martin Biel und Prof. Dr. Christian Wahl von der Ludwig-Maximilians-Universität (LMU) München sowie den Virologen Dr. Robert Davy vom Texas Biomedical Research Institute in San Antonio/USA in der aktuellen Ausgabe des Wissenschaftsmagazins Science.
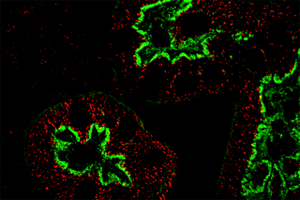
Verteilung von TPC-Kanälen (rot markiert) in Nierenzellen. Bild Quelle: AG Klugbauer/Universität Freiburg
Die Viruserreger docken an Rezeptoren an der Oberfläche von Makrophagen, den Fresszellen des Immunsystems, an. Das löst eine Kette von Ereignissen aus: Die Zellen umschließen die Viren mit Ausstülpungen und fangen sie so in Vesikeln ein, die wiederum mit anderen Vesikeln, den Lysosomen, verschmelzen. Bei diesem Zusammenschluss spielen bestimme Ionenkanäle in den Membranen der Vesikel, so genannte Two Pore Channels (TPC-Kanäle), eine wichtige Rolle. Diese Kanäle, so fanden die Forschenden jetzt heraus, sind für den Infektionsweg der Viren unerlässlich, da sie das nötige Calcium-Ionen-Signal liefern. Sind sie blockiert oder defekt, bleiben die Viren in den Vesikeln stecken und der Infektionszyklus wird wirkungsvoll unterbrochen.
Die Arbeitsgruppe um Klugbauer untersuchte die TPC-Kanäle, die in nahezu allen Zellen des menschlichen Körpers vorhanden sind. Den Freiburger Forschenden gelang es, Zellen so zu verändern, dass sie keine TPC-Kanäle mehr bilden können. An diesen Zellen untersuchten sie, welche Konsequenzen das Fehlen dieser Kanäle zur Folge hat. Es zeigte sich, dass TPC-Kanäle für intrazelluläre Transportprozesse zentral sind: Bestimmte Proteine können ohne die Kanäle innerhalb der Zelle nur verzögert an ihren Zielort gelangen oder auch schlechter abgebaut werden. Genau diese intrazellulären Wege nutzen auch Ebolaviren, um Zellen zu infizieren. Die in Freiburg veränderten Zellen bilden daher die Grundlage für die Untersuchungen zur Aufnahme und zellulären Verbreitung der Ebolaviren.
Klugbauer ist Arbeitsgruppenleiter am Institut für Experimentelle und Klinische Pharmakologie und Toxikologie der Albert-Ludwigs-Universität Freiburg und Projektleiter im Transregio-Sonderforschungsbereich 152 „Steuerung der Körper-Homöostase durch TRP-Kanal-Module“, dessen Sprecheruniversität die LMU München ist.
Originalpublikation: Yasuteru Sakurai, Andrey A. Kolokoltsov, Cheng-Chang Chen, Michael W. Tidwell, William E. Bauta, Norbert Klugbauer, Christian Grimm, Christian Wahl-Schott, Martin Biel, Robert A. Davey. 2015. Two pore channels control Ebolavirus host cell entry and are drug targets for disease treatment. Science. www.sciencemag.org/content/347/6225/995
Doi: 10.1126/science.1258758
*Source: Universität Freiburg
