Wissenschaftler der Universität Tübingen entdecken, wie der Körper das Alarmsignal Chitin erkennt
Chitin stützt die Zellwand von Pilzen, wie zum Beispiel dem Schimmelpilz Aspergillus und der Hefe Candida, die beide gefährliche Infektionen beim Menschen hervorrufen können. Chitin bildet auch das Außenskelett von Insekten und Spinnentieren, zu denen die Milben gehören, und ist daher wichtiger Bestandteil von Hausstauballergenen.
In Säugetieren selbst kommt Chitin nicht vor, sodass das Immunsystem des Menschen den Naturstoff als körperfremd erkennen und mit Abwehrmaßnahmen darauf reagieren sollte. Bisher ließ sich eine direkte Bindung von Chitin an einen Rezeptor des Immunsystems jedoch nicht belegen. Einem internationalen Forscherteam unter der Leitung von Professor Alexander Weber vom Interfakultären Institut für Zellbiologie der Universität Tübingen ist es nun gelungen, einen Rezeptor der angeborenen Immunabwehr als Chitinsensor zu identifizieren. Die Aufklärung der Chitin-Rezeptor-Bindung bietet Angriffsziele für die Entwicklung neuer Therapien für Erkrankungen und Infektionen, die mit Chitin in Verbindung stehen. Die Ergebnisse werden in der Fachzeitschrift EMBO Reports veröffentlicht.
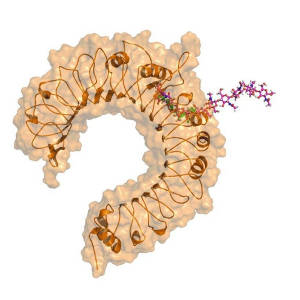
3D-Computer-Modell des TLR2-Rezeptors (orange), der eine Chitinkette (pink) bindet. Dabei passen 5 Chitin-Untereinheiten in die Bindetasche von TLR2, mit der dieser Rezeptor auch andere Muster, die auf Pathogene hindeuten, erkennen kann. Der Teil der Chitinkette, der aus dem Rezeptor herausragt, wird vermutlich benötigt, um einen zweiten Rezeptor zu vernetzen, was zur Aktivierung einer Signalkette und damit zu Immun- und Entzündungsreaktionen führt. Image credit: © Alexander Weber
Nach Zellulose, dem Hauptbestandteil der pflanzlichen Zellwände, gilt Chitin als das zweithäufigste natürliche Polysaccharid, auch Vielfachzucker genannt. Chitin besteht aus flexiblen Ketten oder Flächen des immer gleichen Grundbausteins, der in den Zellwänden der Pilze oder im Außenskelett von Tieren zu steifen Strukturen vernetzt wird. Partikel um einen Millimeter aktivieren das Immunsystem nicht, doch tausendmal kleinere Teilchen im Mikrometerbereich sind seit langem als Immunaktivatoren bekannt. „In bisherigen Experimenten zur Immunerkennung von Chitin wurden zwar häufig Mikrometerpartikel verwendet. Diese waren jedoch teilweise verunreinigt und immer noch größer als eine menschliche Zelle, geschweige denn als ein winziger einzelner Rezeptor“, sagt Alexander Weber. Folglich habe Unklarheit darüber bestanden, wodurch genau eine Immunreaktion ausgelöst wurde.
Bei seinen Experimenten verwendete das Forscherteam daher nun erstmals sehr viel kleinere Chitinmoleküle in definierter Zusammensetzung und Größe. Die Experimente ergaben, dass das Chitin aus mindestens sechs Untereinheiten bestehen muss, damit es den Rezeptor des Immunsystems (Toll-ähnlicher Rezeptor TLR2) aktivieren und so die Immunreaktion in Gang setzen kann. „Wir waren überrascht, dass Chitinketten aus fünf oder weniger Grundbausteinen keine Immunreaktion auslösten und möglicherweise sogar die Immunreaktion mildern können“, sagt Weber. Dies sei das Ergebnis für die Chitinsensoren nicht nur beim Menschen und der Maus, „sondern diese Größenabhängigkeit gibt es erstaunlicherweise sogar bei Pflanzen, wie unsere Kollegen in der Pflanzenbiochemie feststellen konnten“.
Ansatzpunkt für Therapien
Neben Pilzinfektionen ist auch die Hausstauballergie eine wirtschaftlich gesehen wichtige Erkrankung, die mit Chitin in Zusammenhang steht. Das eigentliche Allergen ist der Kot der Hausstaubmilbe, auf den viele Menschen mit Atemwegsentzündungen bis hin zu allergischem Asthma reagieren. „Vermutlich fördern Stoffe wie Chitin die Immunreaktion gegen diese Ausscheidungsprodukte, ähnlich wie ein Impfstoff, der das Immunsystem auf ein bestimmtes Antigen ‚scharf‘ macht“, sagt der Wissenschaftler. Bei einer Pilzinfektion sei es gut, wenn das Immunsystem durch Chitin aktiviert wird. Definierte Chitinketten könnten möglicherweise in Impfstoffen Verwendung finden. Anders bei der Hausstaubmilbe, die vergleichsweise harmlos ist für den Menschen: Die allergische Erkrankung entsteht durch eine Überreaktion des Immunsystems, zu der das im Hausstaub enthaltene Chitin beiträgt. Sie sollte unterdrückt werden.Blockierten die Forscher im Experiment die Bindung von Chitin an den Rezeptor TLR2, folgte keine durch das Chitin vermittelte Entzündung, das Immunsystem wurde also nicht alarmiert. „Für beide Zwecke, die Stärkung der Immunreaktion gegen krankheitserregende Pilze als auch die potenzielle Verhinderung der Immunreaktion gegen Hausstaubmilben, haben wir mit dem Chitin-Rezeptor TLR2 eine wichtige Ansatzstelle gefunden“, fasst Weber zusammen. Bis zur Nutzung dieses Wissens für gezielte Therapien sei es jedoch noch ein weiter Weg.
Publikation:
Katharina Fuchs, Yamel Cardona Gloria, Olaf-Oliver Wolz, Franziska Herster, Lokesh Sharma, Carly A. Dillen, Christoph Täumer, Sabine Dickhöfer, Zsofia Bittner, Truong-Minh Dang, Anurag Singh, Daniel Haischer, Maria A. Schlöffel, Kirsten J. Koymans, Tharmila Sanmuganantham, Milena Krach, Thierry Roger, Didier Le Roy, Nadine A. Schilling, Felix Frauhammer, Lloyd S. Miller, Thorsten Nürnberger, Salomé LeibundGut-Landmann, Andrea A. Gust, Boris Macek , Martin Frank, Cécile Gouttefangeas, Charles S. Dela Cruz, Dominik Hartl, Alexander N.R. Weber: The fungal ligand chitin directly binds TLR2 and triggers inflammation dependent on oligomer size. EMBO Reports, 10.15252/embr.201846065, embor.embopress.org/cgi/doi/10.15252/embr.201846065.
*Source: Universität Tübingen
